11. Disinfezione delle acque
11. Disinfezione delle acque
La disinfezione è l'ultimo step di depurazione delle acque.
La disinfezione delle acque è il processo che ha l'obiettivo di rimuovono gli agenti patogeni che causano malattie infettive in un organismo ospite prima di sversare le acque nell'ambiente.
Si differenzia dalla sterilizzazione, che ha invece l'obiettivo di eliminare qualsiasi microrganismo.
Alla luce di questa differenza, si dice che la disinfezione opera in maniera SELETTIVA.
Nelle tabelle sono mostrati i principali agenti patogeni con le malattie che provocano:

Di particolare interesse sono:
- Escherichia Coli
- Salmonella
che sono quelli le cui concentrazioni sono in genere superiori alla dose infettiva.
Teoria della disinfezione
Caratteristiche degli agenti disinfettanti
Idealmente, un agente disinfettante dovrebbe possedere le caratteristiche presentate nella tabella sottostante:
| Caratteristica | Proprietà |
|---|---|
| Disponibilità | Dovrebbe essere disponibile in grandi quantità e a un prezzo ragionevole |
| Capacità di deodorizzazione | Dovrebbe rimuovere gli odori durante la disinfezione |
| Omogeneità | La soluzione dovrebbe possedere una concentrazione uniforme |
| Interazione con materiali estranei | Non dovrebbe essere assorbito da sostanza organica e altre cellule batteriche |
| Non corrosivo o macchiante | Non dovrebbe alterare metalli o rivestimenti in acciaio |
| Assenza di tossicità per forme di vita superiori | Dovrebbe risultare tossico solo per i microrganismi ma non per animali o esseri umani |
| Penetrazione | Capacità di penetrare attraverso le superfici |
| Sicurezza | Sicuro da trasportare, stoccare, manipolare e utilizzare |
| Solubilità | Solubilità in acqua o nel tessuto cellulare |
| Stabilità | Mantenere il potere germicida inalterato nel tempo |
| Tossicità verso i microrganismi | Efficace a elevate diluizioni |
| Tossicità a temperatura ambiente |
Metodi di disinfezione
Ci sono svariati tipi di processi di disinfezione:
- Meccanici
- Filtrazione
- 6. Sedimentazione
- Fisici
- Calore
- Onde sonore
- Radiazioni ultraviolette
- Radiazioni gamma
- Chimici
- Sostanze ossidanti (
e composti, ) --> vd. #Clorazione - Saponi e detergenti sintetici
- Acidi e basi
- Alcoli
- Composti fenolici
- Metalli pesanti e relativi composti
- Sostanze ossidanti (
I vari processi di depurazione affrontati hanno un impatto non indifferente nella rimozione degli agenti patogeni, raggiungendo percentuali di rimozione dell'ordine anche del
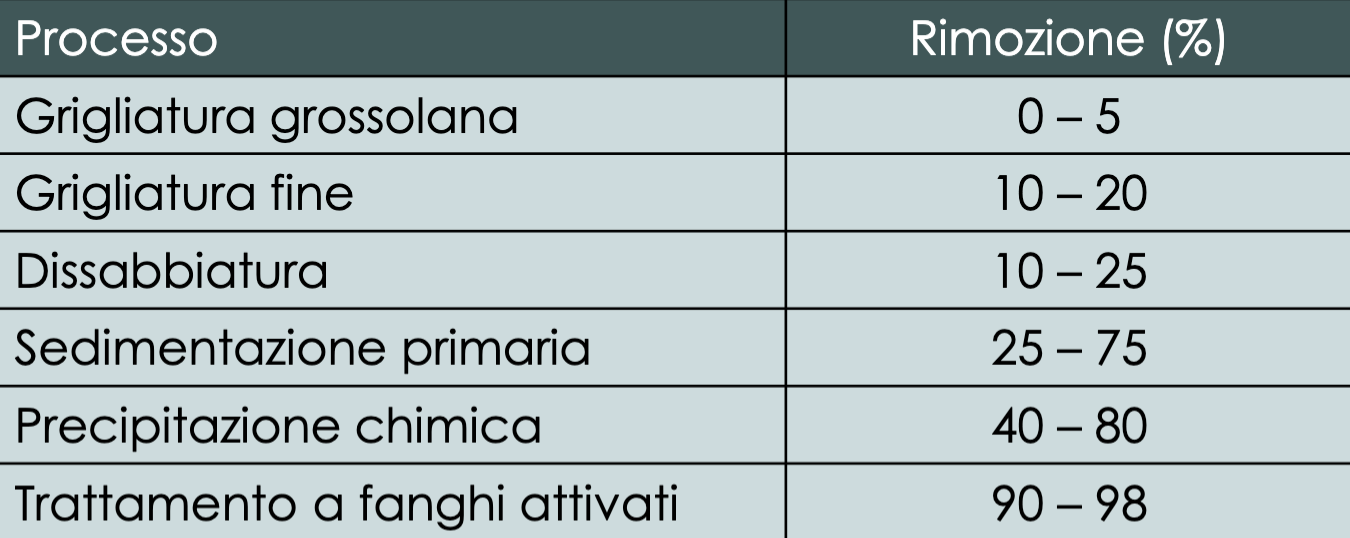
Seppure possa sembrare una percentuale molto elevata, in realtà è comunque insufficiente a scendere sotto la soglia infettiva.
Per questa ragione è necessario un ulteriore step di disinfezione.
Meccanismi di azione dei disinfettanti
I processi di disinfezione sfruttano diversi tipi di meccanismi:
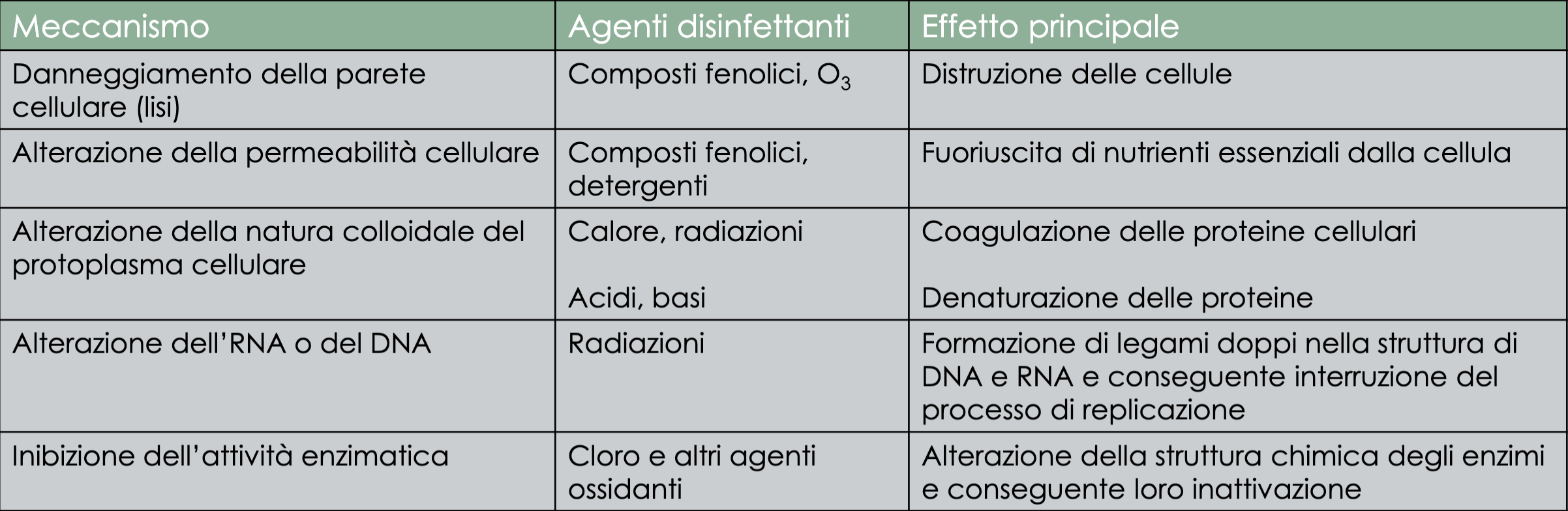
A seguito del processo di disinfezione, possono nascere dei sottoprodotti i quali anche loro andranno rimossi in quanto potrebbero avere effetti negativi:
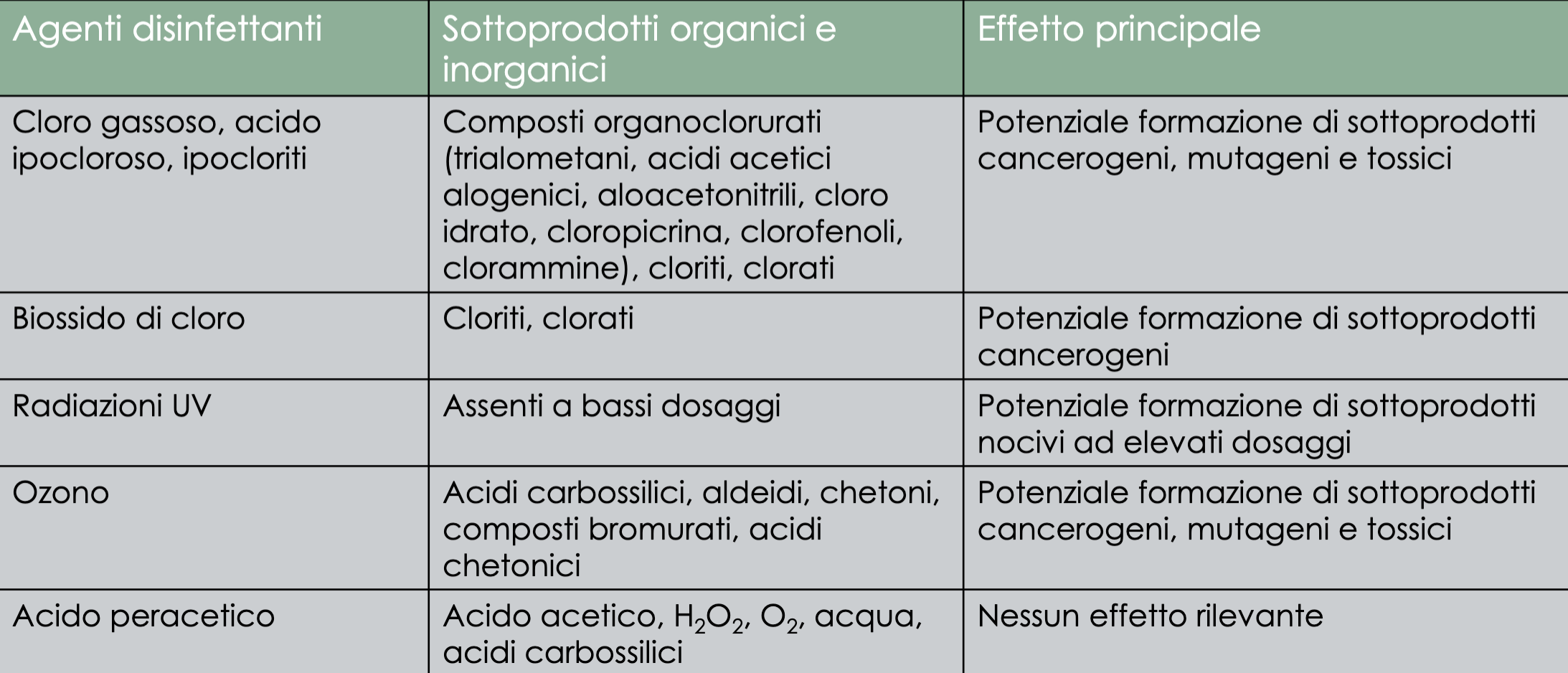
Fattori in grado di influenzare l'azione della disinfezione
L'efficacia della disinfezione è alterata da diversi fattori. In particolare vedremo:
- #Tempo di contatto
- #Concentrazione di disinfettante
Tempo di contatto
Il tempo di contatto rappresenta probabilmente la variabile più rilevante nel processo di Disinfezione delle acque.
La sua influenza fu studiata nei primi del novecento da Harriet Chick.
Le sue osservazioni sono riassunte nella #Legge di Chick:
Legge di Chick
Per una assegnata concentrazione di agente disinfettante, il numero di microrganismi eliminati aumenta al crescere del tempo di contatto.
dove:
Variazione nel tempo del numero di microrganismi costante di velocità di reazione Numero di microrganismi presenti al tempo Tempo
Sia
la quale è linearizzata per mezzo del logaritmo natuarle:
L'andamento della Legge di Chick è mostrato nella figura seguente:
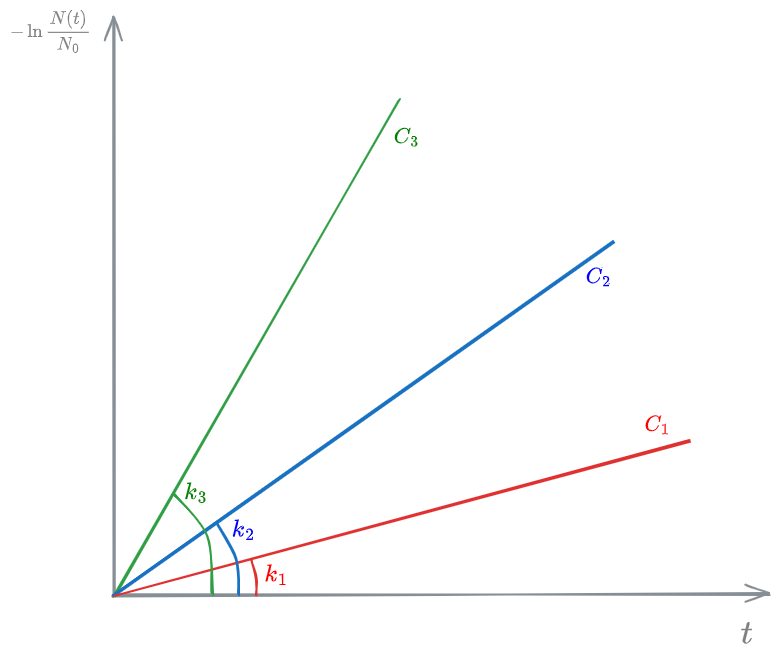
Sono mostrate le curve per 3 valori diversi della costante di velocità. Come vedremo in #Concentrazione di disinfettante, la costante di velocità dipende dalla concentrazione di disinfettante.
L'asse delle ordinate va letto come quantità di agente patogeno rimosso. Più ne viene rimosso, più in alto sarà il valore della quantità
Concentrazione di disinfettante
Legge di Watson
Esiste proporzionalità diretta tra la costante di velocità della #Legge di Chick e la concentrazione di disinfettante elevata al coefficiente di diluizione
dove:
Costante di velocità della [[#Legge di Chick]] Costante di scomparsa dei microrganismi Concentrazione di disinfettante Costante di diluizione
La legge di Watson può essere graficata come segue:
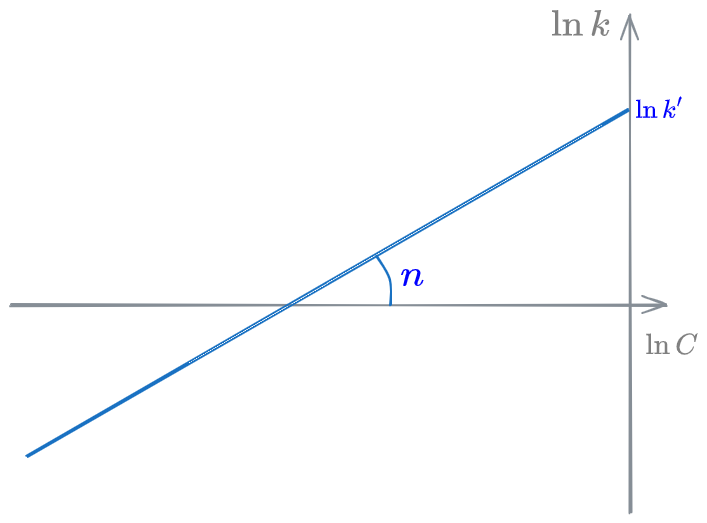
Integrando insieme la #Legge di Watson si ottiene la relazione
Resistenza alla disinfezione
Per individuare l'eventuale contaminazione da agenti patogeni, si fa uso di organismi indicatori della loro presenza. Questi, devono avere un determinato set di caratteristiche:
- Presenza nel caso in cui esista una contaminazione di origine fecale
- Presenza in numero maggiore o uguale a quello dell’organismo patogeno di cui si vuole verificare la presenza
- Capacità di sopravvivenza superiore a quella degli organismi patogeni
- Incapacità a riprodursi al di fuori dell’organismo ospite
- Isolamento e stima quantitativa più rapidi di quelli degli organismi patogeni
- Presenza nella microflora intestinale degli organismi a sangue caldo
Tenute a mente queste caratteristiche, sono solitamente utilizzati: - Coliformi Fecali (come Escherichia Coli...)
- Enterococchi
Diversi patogeni, hanno resistenze diverse agli agenti disinfettanti. Nel diagramma sono mostrati alcuni agenti patogeni in ordine crescente di resistenza:

Uno dei principali metodi di disinfezione è la #Clorazione
Clorazione
- [?] Cosa centra la clorazione con la disinfezione? In tutto il processo di clorazione non ho mai trovato menzione di agenti patogeni
Il Cloro è uno dei disinfettanti di tipo chimico più largamente usato nella Disinfezione delle acque. Questo difatti soddisfa la maggior parte delle #Caratteristiche degli agenti disinfettanti ideali.
Caratteristiche dei composti del cloro
Ci sono diverse forme di cloro che vengono utilizzate:
- #Cloro elementare - Ipoclorato di calcio e di sodio - Biossido di Cloro
Cloro elementare
Reazioni del cloro
Ci sono 2 reazioni diverse che coinvolgono il cloro:
- #Idrolisi del Cloro
- #Dissociazione dell'acido ipocloroso
Il cloro ha potere disinfettante solo se si ossida, riducendo qualcos'altro. Pertanto, il
Idrolisi del Cloro
In cui
- Si ossida ad Acido ipocloroso (
) - Si riduce a
La stessa specie si ossida e si riduce. Si parla pertanto di disproporzione.
A questa reazione è associata una costante di idrolisi:
dove
L'elevato valore della costante di equilibrio mostra come grandi quantità di cloro possano essere disciolte in acqua.
Dissociazione dell'acido ipocloroso
L'Acido ipocloroso si dissocia in ioni
A questa reazione è associata come costante di reazione:
Potere disinfettante del cloro
Abbiamo detto che ci sono varie forme in cui possiamo trovare il #Cloro elementare disciolto in acqua. Principalmente:
È di nostro particolare interesse conoscere la #Distribuzione relativa delle specie di cloro in quanto non tutte le specie di cloro hanno lo stesso potere disinfettante. In particolare, l'Acido ipocloroso ha un potere disinfettante
È inoltre importante menzionare che il cloro agisce da disinfettante solo nel caso in cui si ossidi. Questo esclude il
Distribuzione relativa delle specie di cloro
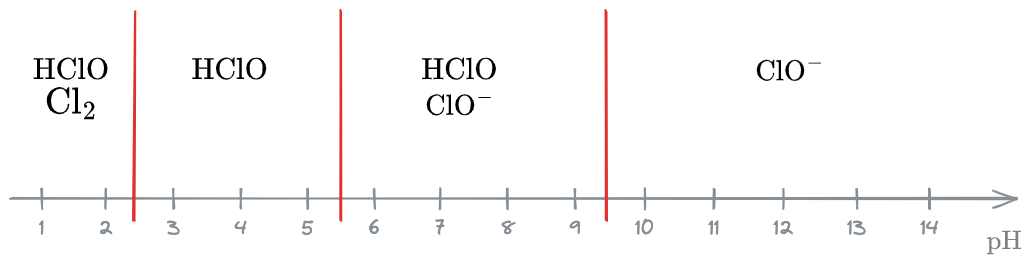
Campo di esistenza dello ione ipoclorito
Cerchiamo di capire in che condizioni troviamo maggiori concentrazioni di Ione Ipoclorito.
Cerchiamo cioè in che condizioni la reazione che segue è spostata principalmente verso destra:
Si avrà prevalenza di
Ricordando la costante di #Dissociazione dell'acido ipocloroso, il rapporto sopra si può scrivere come:
Calcolo il logaritmo a entrambi i membri:
ossia:
Campo di esistenza dell'acido ipocloroso
Cerchiamo di capire in che condizioni troviamo maggiori concentrazioni di Acido ipocloroso (indissociato)
Cerchiamo cioè in che condizioni la reazione che segue è spostata principalmente verso sinistra:
Si avrà prevalenza di
Ricordando la costante di #Dissociazione dell'acido ipocloroso, il rapporto sopra si può scrivere come:
Calcolo il logaritmo a entrambi i membri:
ossia
Confronto tra
Vediamo anche in che condizione si ha prevalenza di Acido ipocloroso rispetto al cloro gassoso (
Cerchiamo cioè quando la concentrazione di
Ricordando la costante di #Idrolisi del Cloro:
Calcolo il logaritmo a entrambi i membri (tenendo conto che solitamente
ossia
Interazioni tra Cloro e sostanze in fase liquida
Alcune sostanze che si trovano in fase liquida possono interferire con l'azione disinfettante del cloro. Queste sono infatti sostanze che si ossidano riducendo il cloro e rendendolo una specie inefficace ai fini della Disinfezione.
Ad esempio:
- Sostanze inorganiche riducenti:
- Composti organici instauri, Solforati o policiclici con gruppi funzionali ossidrile
- Azoto ammoniacale
Reazioni del cloro con Ammoniaca
I reflui non trattati contengono Azoto in forma di ammoniaca nonché legato a diversi composti di natura organica.
Qualora sia presente un'unità di nitrificazione all'interno di un impianto di depurazione, è facile che l'effluente contenga quantità rilevanti di azoto ammoniacale o in forma di nitrati.
Essendo l'Acido ipocloroso un agente estremamente ossidante, esso, in presenza di azoto ammoniacale, tende a reagire andando a formare le cosiddette clorammine.
Questo avviene secondo la seguente successione di reazioni:

Nella maggior parte dei casi prevalgono la Monoclorammina (
Nelle reazioni di formazione delle clorammine e del tricloruro di azoto il cloro non cambia numero di ossidazione. Il cloro nelle clorammine pertanto è ancora cloro in grado di ossidarsi e quindi di agire da disinfettante.
Quindi, il cloro presente nella forma di monoclorammine e diclorammine è detto #Cloro disponibile combinato.
Le clorammine in effetti fungono anche da agenti disinfettanti, sebbene la loro azione si esplichi lentamente nel tempo.
Qualora le clorammine fossero gli unici agenti disinfettanti presenti, il #Cloro residuo misurato viene detto #Cloro combinato residuo per distinguerlo dal #Cloro libero nelle forme di Acido ipocloroso e Ione Ipoclorito.
Cloro disponibile
Il cloro disponibile, o cloro residuo, è il cloro che, a seguito di eventuali reazioni. cheavvengono nel liquido, rimane capace di ossidarsi e quindi di agire da agente disinfettante
Include pertanto:
- #Cloro elementare
- Cloro gassoso - Acido ipocloroso - Ione Ipoclorito
- Cloro combinato (clorammine)
NON include:
-
-
[?] Perché il #Cloro elementare, se aggiunto in soluzione, si trasforma tutto in
se nella reazione di #Idrolisi del Cloro abbiamo visto che in realtà una parte diventa Acido ipocloroso?
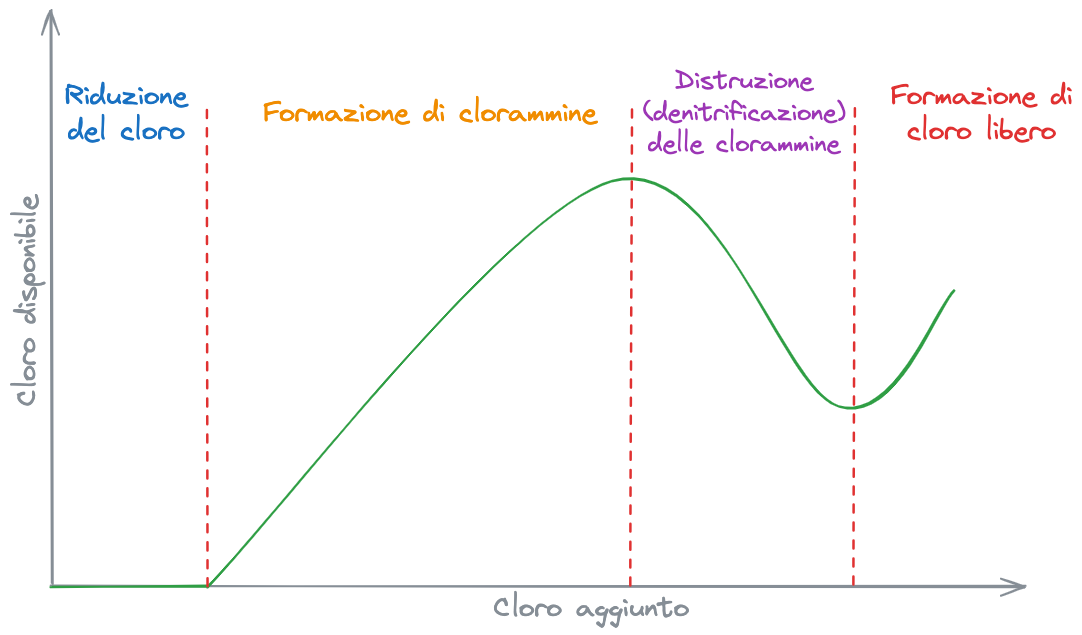
Riduzione del cloro
In una prima fase, appena viene introdotto, il cloro agisce da agente ossidante. Ossida sostanze quali
- Sostanze inorganiche:
Queste sono sostanze interferenti in quanto tolgono cloro disponibile alla soluzione.
In questa fase quindi, tutto il cloro si riduce, e in soluzione non troveremo cloro disponibile alla Disinfezione delle acque.
Formazione delle clorammine
Dopo aver ossidato tutte le sostanze organiche riducenti, il cloro inizia a formare clorammine. Queste costituiscono #Cloro disponibile.
In questa fase, tutto il cloro che aggiungo, lo ritrovo come cloro disponibile. L'andamento sul grafico in questo tratto è di fatto quello di una retta a 45°. Questo è vero a meno che in soluzione sia presente, oltre all'azoto ammoniacale, sostanze del secondo tipo (Composti organici instauri, Solforati o policiclici con gruppi funzionali ossidrile), non trovo più una retta a 45° ma una pendenza più bassa. In quanto una parte di cloro che aggiungo va in
Distruzione (denitrificazione) delle clorammine
A questo punto ho formato tutte le possibili clorammine e saturato tutti i possibili composti organici. Dal punto di massimo in poi, la curva decresce. Aggiungo cloro ma ne trovo di meno.
Le clorammine possono ulteriormente trasformarsi. Possono infatti tornare a reagire col cloro:
- Possono reagire con l'Acido ipocloroso:
- Possono reagire tra di loro (denitrificazione delle clorammine):
Nelle ultime reazioni descritte si noti che il cloro si riduce. Il cloro ridotto non agisce più come agente ossidante. Non verrà quindi contato come cloro disponibile.
Per questo motivo, il cloro che aggiungo non lo ritrovo come cloro disponibile e la curva decresce.
In linea teorica la curva dovrebbe arrivare a zero, avendo consumato tutte le clorammine che si erano formate nella fase precedente. Nella realtà non si arriva mai a zero perché c'è sempre qualche composto più complesso che rimane come cloro disponibile.
Formazione di cloro libero
Dal punto di minimo in poi, non essendoci più nulla che può reagire col cloro, tutto quello che aggiungo rimane come cloro disponibile alla disinfezione. Inoltre si tratta tutto di cloro libero.
Inoltre, il punto di minimo, si chiama breakpoint e indica la dose di cloro necessaria a consumare tutte le sostanze che interferiscono con la disinfezione per clorazione.
La condizione meno vantaggiosa di tutte è il punto di minimo: dosaggio elevato ma cloro disponibile basso.
Nonostante questo esistono dei processi detti clorazione al breakpoint. Questi sono quei processi per rimuovere l'azoto. La clorazione al breakpoint non c'entra niente con la disinfezione. È un metodo chimico di rimozione dell'azoto.
Ammoniaca e varecchina (cloro) fanno interferenza tra loro.
Dosaggio di cloro:
Esempio con alcol e covid.
All'inizio del Covid si diceva di pulire le superfici usando alcol non al 90% ma diluito almeno al 70%. Questo ha a che fare con il tempo di contatto. L'alcol infatti evapora molto velocemente. Diluito invece ci mette di più ad evaporare e rimane a contatto con il virus più a lungo.
Le clorammine hanno efficacia minore del cloro libero, almeno nell'immediato. In generale però, l'effetto disinfettante del cloro combinato dura di più. Un potere disinfettante prolungato può prevenire eventuali ricontaminazioni da agenti patogeni.
A seconda del tipo di effetto desiderato, quando si vuole disinfettare un refluo, ci si metterà in punti diversi della curva:
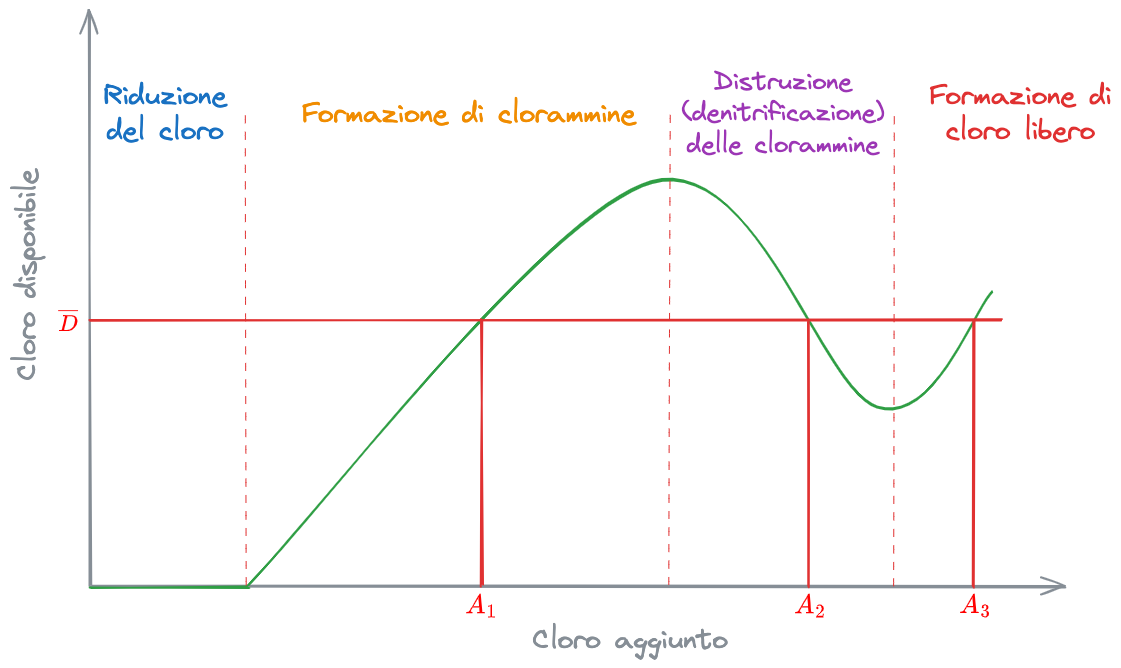
Immaginiamo che, al fine di disinfettare un certo refluo, abbiamo necessità di avere in soluzione una certa quantità
In corrispondenza di
In corrispondenza di
Rimozione del cloro residuo
A valle della #Clorazione può essere necessario rimuovere il cloro eventualmente residuo dal processo di disinfezione in quanto questo può essere tossico per le specie organiche in natura.
Andranno usate specie riducenti, per ridurre il cloro che è in forma ossidata.
Agenti chimici maggiormente utilizzati - composti riducenti:
- Biossido di zolfo (
) - Solfito di sodio (
) - Bisolfito di sodio (
) - Metabisolfito di sodio (
) - Tiosolfato di sodio (
)